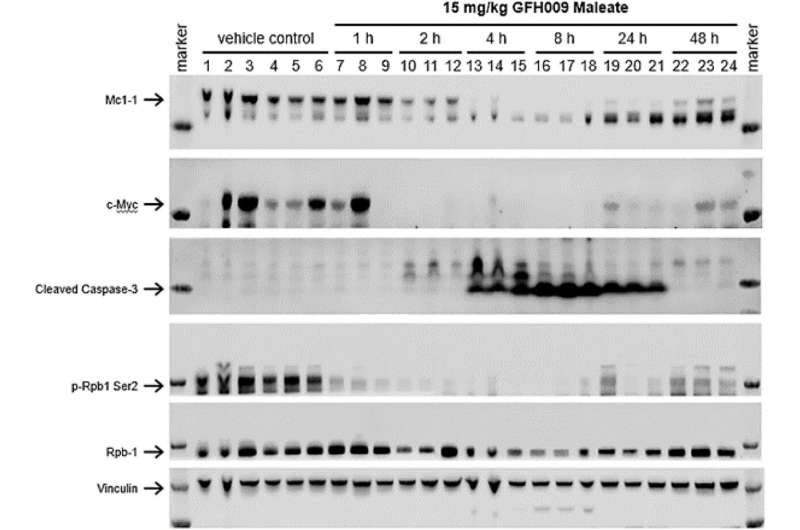
Wirkung der GFH009-Behandlung auf die CDK9-abhängige Proteinexpression in vivo. Bildnachweis: 2023 Zhou et al
Um den Kontrollen des Zellzyklus zu entgehen, sind bösartige Zellen auf die schnelle Expression ausgewählter Proteine angewiesen, um proapoptotische Signale abzuschwächen, die aus Schäden resultieren, die sowohl durch Krebsbehandlungen als auch durch unkontrollierte Überproliferation verursacht werden. Die von Cyclin-abhängiger Kinase 9 (CDK9) abhängige Signalübertragung induziert die Transkription nachgeschalteter Onkogene und fördert das Tumorwachstum, insbesondere bei hyperproliferativen „onkogenabhängigen“ Krebsarten wie humanen hämatologischen Malignomen (HHMs).
In einer neuen Studie veröffentlicht in Oncotarget Mit dem Titel „Die pharmakodynamische und mechanistische Grundlage für die antineoplastischen Effekte von GFH009, einem wirksamen und hochselektiven CDK9-Inhibitor zur Behandlung hämatologischer Malignome“ wollten Forscher von GenFleet Therapeutics Inc. und der Sellas Life Sciences Group das aktuelle Wissen zusammenfassen, das dem Wirkmechanismus zugrunde liegt (MOA) von GFH009 und erklären seine robuste Antikrebsaktivität.
„Das Verständnis des MOA von GFH009 ermöglicht einen optimaleren klinischen Entwicklungspfad, da das Potenzial für bedeutende Vorteile bei Patienten mit hämatologischen Malignomen besteht“, erklären die Forscher.
GFH009, ein wirksamer, hochselektiver CDK9-Inhibitor kleiner Moleküle, zeigte antiproliferative Aktivität in verschiedenen HHM-abgeleiteten Zelllinien und induzierte Apoptose bei IC50-Werten unter 0,2 μM in 7/10 getesteten Linien. GFH009 hemmte das Tumorwachstum bei allen Dosen im Vergleich zu den Kontrollen und induzierte dosisabhängig Apoptose.
Zweiwöchentliche Injektionen von 10 mg/kg GFH009-Maleat verlängerten das Überleben von MV-4-11-Xenotransplantat-tragenden Nagetieren signifikant, während ihr Körpergewicht stabil blieb. Nach der Arzneimittelexposition kam es sowohl in vitro als auch in vivo zu einer deutlichen Verringerung der MCL-1- und c-MYC-Proteinexpression. Durch die schnelle „Ein-Aus“-Hemmung von CDK9 übt GFH009 eine proapoptotische Wirkung auf präklinische HHM-Modelle aus, die durch den dynamischen Entzug entscheidender Zellüberlebenssignale ausgelöst wird.
„Unsere Ergebnisse belegen mechanistisch, dass CDK9 eine angreifbare Schwachstelle in verschiedenen HHMs ist, und zusammen mit der zuvor gezeigten überlegenen Kinomselektivität von GFH009 im Vergleich zu anderen CDK9-Inhibitoren unterstützen sie nachdrücklich die Gründe für derzeit laufende klinische Studien mit diesem Wirkstoff bei akuter myeloischer Leukämie und anderen.“ „HHMs“, behaupten die Forscher.
Mehr Informationen:
Fusheng Zhou et al., Die pharmakodynamische und mechanistische Grundlage für die antineoplastischen Wirkungen von GFH009, einem wirksamen und hochselektiven CDK9-Inhibitor zur Behandlung hämatologischer Malignomen, Oncotarget (2023). DOI: 10.18632/oncotarget.28543
Bereitgestellt von Impact Journals LLC
Zitat: Wirksamer und hochselektiver CDK9-Inhibitor zur Behandlung hämatologischer Malignome (2023, 29. Dezember), abgerufen am 31. Dezember 2023 von https://medicalxpress.com/news/2023-12-potent-highly-cdk9-inhibitor-treatment.html
Dieses Dokument unterliegt dem Urheberrecht. Abgesehen von einem fairen Handel zum Zweck des privaten Studiums oder der Forschung darf kein Teil ohne schriftliche Genehmigung reproduziert werden. Der Inhalt dient ausschließlich Informationszwecken.
